Inducción asimétrica
En estereoquímica, la inducción asimétrica (también enantioinducción) en una reacción química describe la formación preferencial de un enantiómero o diastereómero sobre el otro, como resultado de la influencia de una característica quiral presente en el sustrato, reactivo, catalizador o ambiente.[1] La inducción asimétrica es un elemento clave en la síntesis asimétrica.
La inducción asimétrica fue introducida por Emil Fischer, basado en su trabajo sobre los carbohidratos.[2] Existen varios tipos de inducción.
La inducción asimétrica interna hace uso de un centro quiral unido al centro reactivo por medio de un enlace covalente, y permanece así durante la reacción. En la inducción asimétrica por relay la información quiral es introducida en un paso separado, y eliminado nuevamente en una reacción química separada. Los sintones especiales son denominados auxiliares quirales. En la inducción asimétrica externa, la información quiral es introducida en el estado de transición a través de un catalizador o ligando quiral. Este método de síntesis asimétrica es económicamente el más deseable.
Inducción asimétrica carbonilo 1,2
[editar]Existen varios modelos para describir la inducción quiral en los carbonos carbonílicos durante adiciones nucleofílicas. Estos modelos están basados en una combinación de combinaciones estéricas y electrónicas y suelen ser consideradas en conflicto una con otra. Estos modelos fueron devisados por Cram (1952), Cornforth (1959), Felkin (1969) y otros.
Regla de Cram
[editar]La regla de Cram de la inducción asimétrica, desarrollada por Donald J. Cram en 1952[3] es un concepto inicial relativo a la predicción de la estereoquímica en ciertos sistemas acíclicos. En un todo, la regla es:
En ciertas reacciones no catalíticas, predominará el diastereómero que pueda formarse por la aproximación del grupo entrante desde el lado menos impedido, cuando la conformación rotacional del enlace C-C sea tal que el enlace doble esté flanqueado por los dos grupos menos voluminosos unidos al centro asimétrico adyacente.
La regla indica que la presencia de un centro asimétrico en una molécula induce la formación de un centro asimétrico adyacente a él, basado en el impedimento estérico.
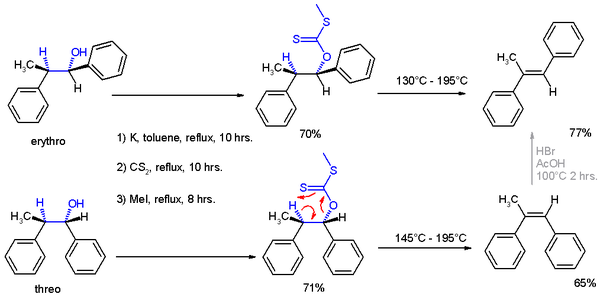
En su publicación de 1952, Cram presentó un gran número de reacciones descritas en la literatura para el que la conformación de los productos de la reacción podría ser explicado sobre la base de su regla, y también describió un experimento elaborado (esquema 1) haciendo su caso.
Los experimentos involucraron dos reacciones. En el experimento uno, el 2-fenilpropionaldehído (1, racémico pero se muestra el enantiómero (R)) reaccionó con el reactivo de Grignard del bromobenceno para formar 1,2-difenil-1-propanol (2) como una mezcla de diastereómeros, predominántemente el isómero treo (ver proyección de Fischer).
La preferencia por la formación del isómero treo puede ser explicada por la regla indicada anteriormente, al tener el nucleófilo activo en esta reacción atacando al grupo carbonilo desde el lado menos impedido (ver la proyección de Newman A) cuando el carbonilo está posicionado en una formación alternada con el grupo metilo y el átomo de hidrógeno, que son los dos sustituyentes más pequeños, creando un mínimo de impedimento estérico, en una orientación gauche y el fenilo como el grupo más voluminoso en la conformación anti.
La segunda reacción es la reducción orgánica de la 1,2-difenil-1-propanona 2 con hidruro de aluminio y litio, lo que resulta en el mismo producto de reacción que arriba, pero con preferencia por el isómero eritro (2a). Ahora, un anión hidruro (H-) es el nucleófilo atacando desde el lado menos impedido.
En la publicación original de 1952 se obtuvo evidencia adicional para asignar estructuras de los productos de reacción, aplicándoles una eliminación de Chugaev, puesto que el isómero treo reacciona para dar el isómero cis del -α-metil-estilbeno y el isómero eritro conduce a la versión trans.
Modelo de Felkin
[editar]El modelo de Felkin (1968) nombrado así en honor a Hugh Felkin, también predice la estereoquímica de las reacciones de adición nucleofílica a grupos carbonilo.[4] Felkin argumentó que el modelo de Cram sufría un gran defecto: una conformación eclipsada en el estado de transición entre el sustituyente en el carbonilo α (el átomo de hidrógeno en el caso de los aldehídos) y el sustituyente más grande β-carbonílico. Demostró que, al aumentar el volumen estérico del sustituyente α desde metilo a etilo a isopropilo a isobutilo, la estereoselectividad también se incrementaba, lo que no estaba predicho por la regla de Cram:
Las reglas de Felkin son:
- Los estados de transición son similares a los reactantes.
- La tensión torsional (tensión de Pitzer) involucrando enlaces parciales (en los estados de transición) representa una fracción sustancial de la tensión entre enlaces completamente formados, incluso cuando el grado de enlace es relativamente pequeño. La conformación en el estado de transición es alternada y no eclipsada con el sustituyente R skew con respecto a los dos grupos adyacentes, uno de ellos es el más pequeño en el estado de transición A.
- En comparación, el estado de transición B es el estado de transición de Cram.
- Las principales interacciones estéricas involucran aquellas alrededor de R y el nucleófilo, pero no el átomo de oxígeno carbonílico.
- Un efecto polar o efecto electrónico estabiliza un estado de transición con máxima separación entre el nucleófilo y un grupo que atrae electrones. Por ejemplo, las halocetona no obedecen la regla de Cram y, en el ejemplo anterior, al reemplazar el grupo fenilo que atrae electrones, por un grupo ciclohexilo se reduce la estereoselectividad considerablemente.
Modelo de Felkin-Anh
[editar]El modelo de Felkin-Anh es una extensión del modelo de Felkin, que incorpora mejoras sugeridas por N. T. Anh y O. Eisenstein para corregir dos debilidades claves en el modelo de Felkin. La primera debilidad señalada fue la indicación hecha por Felkin de un efecto polar fuerte en los estados de transición de la adición nucleofílica, lo que conduce a la inversión completa de la estereoquímica por las reacciones SN2 reactions, sin ofrecer justificaciones por qué se observaba el fenómeno. La solución de Anh era ofrecer el efecto antiperiplanar como una consecuencia de la inducción asimétrica que está siendo contrlada tanto por efectos del sustituyente como por efectos de orbitales.[5][6] En este efecto, el mejor aceptor nucleófilo de orbital σ* está alineado paralelo a ambos orbitales π y π* del carbonilo, lo que provee estabilización del anión que se forma.
La segunda debilidad en el modelo de Felkin fue la suposición de la minimización del sustituyente alrededor del carbonilo, R, lo que no podía ser aplicado a los aldehídos.
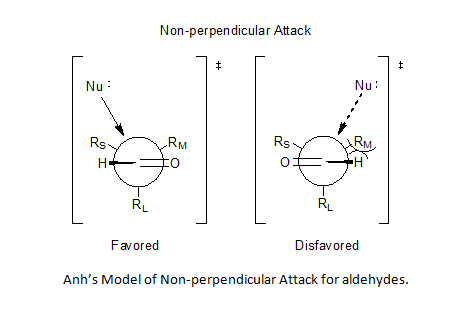
La incorporación de las ideas del ángulo de Bürgi-Dunitz[7][8] le permitieron a Anh postular un ataque no perpendicular por el nucleófilo al centro carbonilo, desde los 95° a los 105° relativos al enlace doble oxígeno-carbono, favoreciendo la aproximación más cercana al sustituyente más pequeño y, en consecuencia, resolviendo el problema de la predictibilidad para los aldehídos.[5][9][10]
Referencias
[editar]- ↑ IUPAC Gold Book definition Link
- ↑ Asymmetric Synthesis of Natural Products, Ari Koskinen ISBN 0-471-93848-3
- ↑ Studies in Stereochemistry. X. The Rule of "Steric Control of Asymmetric Induction" in the Syntheses of Acyclic Systems Donald J. Cram, Fathy Ahmed Abd Elhafez J. Am. Chem. Soc.; 1952; 74(23); 5828-5835. Abstract
- ↑ Torsional strain involving partial bonds. The stereochemistry of the lithium aluminium hydride reduction of some simple open-chain ketones Marc Chérest, Hugh Felkin and Nicole Prudent Tetrahedron Letters Volume 9, Issue 18 , 1968, Pages 2199-2204 doi 10.1016/S0040-4039(00)89719-1
- ↑ a b Anh, N. T.; Eisenstein, O. Nouv. J. Chim. 1977, 1, 61.
- ↑ Anh, N. T.; Eisenstein, O.; Lefour, J-M.; Dau, M-E. J. Am. Chem. Soc. 1973, 95, 6146.
- ↑ Bürgi, H. B.; Dunitz, J. D.; Shefter, E. J. Am. Chem. Soc. 1973, 95, 5065.
- ↑ Bürgi, H. B.; Dunitz, J. D.; Lehn, J. M.; Wipff, G. Tetrahedron 1974, 30, 1563.
- ↑ Anh, N. T.; Eisenstein, O. Tetrahedron Lett. 1976, 155.
- ↑ Anh, N. T. Top. Curr. Chem. 1980, 88, 146.
Enlaces externos
[editar]- The Evolution of Models for Carbonyl Addition Evans Group Afternoon Seminar Sarah Siska February 9, 2001