Diferencia entre revisiones de «Ciclohexanona»
Apariencia
Contenido eliminado Contenido añadido
m Revertidos los cambios de 190.27.35.169 a la última edición de SieBot |
|||
| Línea 79: | Línea 79: | ||
== Referencias == |
== Referencias == |
||
{{listaref}} |
{{listaref}} |
||
[[Categoría:Cetonas]] |
|||
[[de:Cyclohexanon]] |
|||
[[en:Cyclohexanone]] |
|||
[[fi:Sykloheksanoni]] |
|||
[[fr:Cyclohexanone]] |
|||
[[ja:シクロヘキサノン]] |
|||
[[nl:Cyclohexanon]] |
|||
[[pl:Cykloheksanon]] |
|||
[[pt:Cicloexanona]] |
|||
[[ru:Циклогексанон]] |
|||
[[sv:Cyklohexanon]] |
|||
[[zh:环己酮]] |
|||
Revisión del 23:03 30 sep 2009
| Plantilla:Chembox header| Ciclohexanona | |
|---|---|
| |
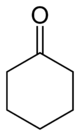
| Nombre IUPAC | Ciclohexanona |
| Otros nombres | Pimelin cetona |
| Fórmula empírica | C6H10O |
| Masa molecular | 98,14 g/mol |
| Estado físico/Color | Líquido/Incoloro |
| Número CAS | 108-94-1 |
| Plantilla:Chembox header | Propiedades | |
| Densidad | 0,9478 g/cm3 a 20 ºC |
| Punto de fusión | -31 °C (242 K) |
| Punto de ebullición | 155,6 °C (428,8 K) |
| Solubilidad en agua | ~90 g/l a 20 ºC |
| Plantilla:Chembox header | Información de Seguridad | |

| |
| Frases R: R10, R20
Frases S: S25 | |
| Plantilla:Chembox header | Exenciones y Referencias[1][2][3][4][5] | |
La ciclohexanona es una molécula cíclica compuesta de seis átomos de carbono y con un grupo funcional cetona. Pertenece por tanto al grupo de las cetonas cíclicas. Es un líquido incoloro, cuyo olor recuerda al de la acetona. La ciclohexanona es solube en agua y miscible con los solventes orgánicos más comunes.
Producción
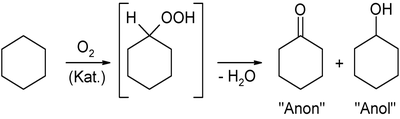
La síntesis industrial de la ciclohexanona tiene lugar principalmente a través de dos procesos:
- Oxidación catalítica de ciclohexano con oxígeno atmosférico, que transcurre a través de un hidroperoxiciclohexano (o hidroperóxido de ciclohexilo) inestable, el cual vía un mecanismo radicalario da lugar a una mezca de ciclohexanona y ciclohexanol, abreviados como ona y ol. La mezcla a continuación se separa por destilación, y el ciclohexanol aislado puede seguidamente oxidarse o deshidrogenarse a más ciclohexanona.
- Hidrogenación catalítica de fenol, con un catalizador de Pd/C.
Reacciones
La ciclohexanona muestra la reactividad típica de una cetona, por ejemplo:
- Forma la imina con amoníaco o aminas primarias.
- Forma la enamina con aminas secundarias.
- Posiciones ácidas en α al grupo carbonilo. Tautomería ceto-enol.
- Reacción aldólica bajo catálisis ácida o básica.
- Reacción con reactivos de Grignard.
- Reacción de Wittig para formar un alqueno.
- Con borohidruro de sodio se reduce con facilidad a ciclohexanol.
Aplicaciones
La ciclohexanona se emplea como disolvente en la industria, y como reactivo en la producción de ácido adípico y de caprolactama, compuestos empleados en la fabricación de nylon-6,6 y nylon-6 respectivamente.

Referencias
- ↑ «Ficha Internacional de Seguridad Química (FISQ)». Consultado el 17 de diciembre de 2008.
- ↑ Acros Organics. «Hoja de Datos de Seguridad (FDS)». Consultado el 17 de diciembre de 2008.
- ↑ Alfa Aesar. «Ficha de datos de seguridad (FDS)». Consultado el 17 de diciembre de 2008.
- ↑ Merck. «Ficha de datos de seguridad (FDS)». Consultado el 17 de diciembre de 2008.
- ↑ Hazardous Substances Data Bank (HSDB)