Diferencia entre revisiones de «Nitrato de potasio»
Sin resumen de edición |
m Revertidos los cambios de 201.102.10.104 a la última edición de 201.206.208.170 |
||
| Línea 2: | Línea 2: | ||
|imagen=[[Archivo:Potassium nitrate.jpg|200px]] |
|imagen=[[Archivo:Potassium nitrate.jpg|200px]] |
||
|IUPAC=Trioxonitrato (V) de potasio |
|IUPAC=Trioxonitrato (V) de potasio |
||
|otros nombres=Nitrato de potasio<br />Nitrato potásico<br />Nitrato de potasa<br />Salitre<br />Nitrato de Chile<br />Sal de Chile |
|otros nombres=Nitrato de potasio<br />Nitrato potásico<br />Nitrato de potasa<br />Salitre<br />Nitrato de Chile<br />Sal de Chile |
||
|masa=101,103 g/mol |
|masa=101,103 g/mol |
||
|fórmula1=[[Potasio|K]][[Nitrato|NO<sub>3</sub>]] |
|fórmula1=[[Potasio|K]][[Nitrato|NO<sub>3</sub>]] |
||
Revisión del 01:29 16 abr 2010
| Nitrato de potasio | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| Trioxonitrato (V) de potasio | ||
| General | ||
| Otros nombres |
Nitrato de potasio Nitrato potásico Nitrato de potasa Salitre Nitrato de Chile Sal de Chile | |
| Fórmula semidesarrollada | KNO3 | |
| Fórmula estructural |
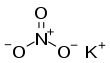 | |
| Fórmula molecular | KNO3 | |
| Identificadores | ||
| Número CAS | 7757-79-1[1] | |
| Número RTECS | TT3700000 | |
| ChEBI | 63043 | |
| ChEMBL | CHEMBL1644029 | |
| ChemSpider | 22843 | |
| DrugBank | DB11090 | |
| PubChem | 139063997, 516903 24434, 139063997, 516903 | |
| UNII | RU45X2JN0Z | |
| KEGG | D02051 | |
| Propiedades físicas | ||
| Apariencia | blanco o gris sucio | |
| Densidad | 2100 kg/m³; 2,1 g/cm³ | |
| Masa molar | 101,103 g/mol g/mol | |
| Punto de fusión | 607 K (334 °C) | |
| Punto de ebullición | 673 K (400 °C) | |
| Estructura cristalina | Ortorrómbico, Aragonita | |
| Propiedades químicas | ||
| Solubilidad en agua | 38 g en 100g de agua | |
| Peligrosidad | ||
| NFPA 704 |
0
1
0
OX
| |
| Riesgos | ||
| Ingestión | Puede causar irritación, náusea, vómitos y diarrea. | |
| Inhalación | Irritación, exposición a largo plazo puede resultar fatal. | |
| Piel | Bajo riesgo. | |
| Ojos | Bajo riesgo. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El compuesto químico nitrato de potasio, salitre, nitrato potásico o nitrato de potasa, nitrato de Chile o sal de Chile es un nitrato cuya fórmula es KNO3-. Actualmente, la mayoría del nitrato de potasio viene de los vastos depósitos de nitrato de sodio en los desiertos Chilenos. El nitrato de sodio es purificado y posteriormente se le hace reaccionar en una solución con cloruro de potasio (KCl), en la cual el nitrato de potasio, menos soluble, cristaliza.
Aplicaciones
Una de las aplicaciones más útiles del nitrato de potasio es la producción de ácido nítrico, añadiendo ácido sulfúrico concentrado a una solución acuosa de nitrato de potasio. Ademas es una reaccion endotermica.
También se usa como fertilizante,se usa en bombas de humo (lo cual es un procedimiento sencillo y sin riesgos.), en las cuales una mezcla con azúcar produce una nube de humo de un volumen 600 veces superior al suyo.
En conservación de alimentos, el nitrato de potasio es un ingrediente poco común de la carne salada. Como conservante es conocido como E252. (Ver aditivos alimentarios).
También es un componente principal en compuestos usados para descomponer con más rapidez restos orgánicos, como los tocones de los árboles, porque acelera el proceso de descomposición.
La creencia popular dice que el nitrato de potasio es un anafrodisíaco, pero en realidad no tiene esa clase de efectos en los humanos.
Finalmente, el nitrato de potasio es el agente oxidante(aporte de oxígeno), componente indispensable de la pólvora. Aunque el nitrato de potasio se usa para producir pólvora, por sí mismo no es combustible ni inflamable.
Es bastante utilizado también para el tratamiento de la hipersensibilidad que afecta a la pulpa dentaria.
Véase también
- Chile, el mayor productor mundial de Nitrato. Además de la falta de Carbono soluble en la superficie del territorio chileno no tuvo gran expansión el nitrato de potasio en la región peruano-boliviana. Las sucesivas guerras de las cuales referimos en la siguiente obra es producto de la producción excesiva del recurso mencionado.

