Diferencia entre revisiones de «Nitroglicerina»
Sin resumen de edición |
Deshecha la edición 36159950 de 186.81.196.75 (disc.) Vandaliz. |
||
| Línea 38: | Línea 38: | ||
|} |
|} |
||
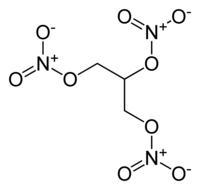
La '''nitroglicerina''', cuyo nombre [[IUPAC]] es 1,2,3-trinitropropano, es un [[éster]] [[química orgánica|orgánico]], que se obtiene mezclando [[ácido nítrico]] concentrado, [[ácido sulfúrico]] y [[glicerina]]. Su [[fórmula molecular]] es [[carbono|C]]<sub>3</sub>[[hidrógeno|H]]<sub>5</sub>[[nitrógeno|N]]<sub>3</sub>[[oxígeno|O]]<sub>9</sub>. El resultado es altamente [[explosivo]]. Es un [[líquido]] a [[temperatura]] ambiente, lo cual lo hace altamente sensible a cualquier movimiento, haciendo muy difícil su manipulación, aunque se puede conseguir una estabilidad |
La '''nitroglicerina''', cuyo nombre [[IUPAC]] es 1,2,3-trinitropropano, es un [[éster]] [[química orgánica|orgánico]], que se obtiene mezclando [[ácido nítrico]] concentrado, [[ácido sulfúrico]] y [[glicerina]]. Su [[fórmula molecular]] es [[carbono|C]]<sub>3</sub>[[hidrógeno|H]]<sub>5</sub>[[nitrógeno|N]]<sub>3</sub>[[oxígeno|O]]<sub>9</sub>. El resultado es altamente [[explosivo]]. Es un [[líquido]] a [[temperatura]] ambiente, lo cual lo hace altamente sensible a cualquier movimiento, haciendo muy difícil su manipulación, aunque se puede conseguir una estabilidad relativa añadiéndole algunas sustancias, como el [[aluminio]]. |
||
Usualmente se transporta en cajas |
Usualmente se transporta en cajas acolchadas a baja temperatura para disminuir el riesgo de explosión, ya que si sobrepasa los 41 °C (temperatura límite estimada) se produce una reacción muy violenta debido a la agitación intermolecular: |
||
<math> |
|||
4 C_3H_5(NO_3)_3 (l) = 12 CO_2(g) + 10 H_2O(g) + O_2(g) + 6 N_2(g)</math> |
|||
Cuando [[Alfred Nobel]] inventó la [[dinamita]], la cual es más segura, disminuyó el uso de la "'''nitro'''" (como también se le llama) para ser reemplazada por el nuevo invento. |
Cuando [[Alfred Nobel]] inventó la [[dinamita]], la cual es más segura, disminuyó el uso de la "'''nitro'''" (como también se le llama) para ser reemplazada por el nuevo invento. |
||
Revisión del 16:03 16 abr 2010
| |||||||||||||||||||||||||||||||
La nitroglicerina, cuyo nombre IUPAC es 1,2,3-trinitropropano, es un éster orgánico, que se obtiene mezclando ácido nítrico concentrado, ácido sulfúrico y glicerina. Su fórmula molecular es C3H5N3O9. El resultado es altamente explosivo. Es un líquido a temperatura ambiente, lo cual lo hace altamente sensible a cualquier movimiento, haciendo muy difícil su manipulación, aunque se puede conseguir una estabilidad relativa añadiéndole algunas sustancias, como el aluminio.
Usualmente se transporta en cajas acolchadas a baja temperatura para disminuir el riesgo de explosión, ya que si sobrepasa los 41 °C (temperatura límite estimada) se produce una reacción muy violenta debido a la agitación intermolecular:
Cuando Alfred Nobel inventó la dinamita, la cual es más segura, disminuyó el uso de la "nitro" (como también se le llama) para ser reemplazada por el nuevo invento.
La nitroglicerina es el componente principal de algunas mezclas explosivas como la abelita compuesta por un 65 % de nitroglicerina, 30 % de algodón pólvora, 3,5 % de salitre y finalmente un 1,5 % de carbonato de sodio.
En medicina, se usa como vasodilatador para el tratamiento de la enfermedad isquémica coronaria, el infarto agudo de miocardio y la insuficiencia cardíaca congestiva. Se administra por las vías oral, transdérmica, sublingual o intravenosa.
Historia
La nitroglicerina fue sintetizada en el año 1846 por el químico italiano Ascanio Sobrero. En 1867, imaginó el célebre Alfred Nobel absorber la nitroglicerina por una materia porosa e inerte como el sílice, polvos de ladrillo, arcilla seca, yeso, carbón, etc. producto que constituye la dinamita.