Diferencia entre revisiones de «Hidróxido de potasio»
Sin resumen de edición |
m Revertidos los cambios de 201.110.149.216 a la última edición de Xqbot |
||
| Línea 1: | Línea 1: | ||
{{Ficha de compuesto químico |
{{Ficha de compuesto químico |
||
Masa molar= 56g/mol |
|||
|IUPAC = Hidróxido de potasio |
|IUPAC = Hidróxido de potasio |
||
|otros nombres = Hidróxido potásico,<br />potasa cáustica |
|otros nombres = Hidróxido potásico,<br />potasa cáustica |
||
Revisión del 23:15 26 abr 2010
| Hidróxido de potasio | ||
|---|---|---|
 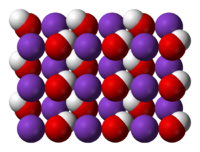 | ||
| Nombre IUPAC | ||
| Hidróxido de potasio | ||
| General | ||
| Otros nombres |
Hidróxido potásico, potasa cáustica | |
| Fórmula semidesarrollada | KOH | |
| Fórmula molecular | KOH | |
| Identificadores | ||
| Número CAS | 1310-58-3[1] | |
| Número RTECS | TT2100000 | |
| ChEBI | 32035 | |
| ChEMBL | CHEMBL2103983 | |
| ChemSpider | 14113 | |
| DrugBank | DB11153 | |
| PubChem | 14797 | |
| UNII | WZH3C48M4T | |
| KEGG | D01168 C12568, D01168 | |
| Propiedades físicas | ||
| Apariencia | Blanco | |
| Densidad | 2000 kg/m³; 2 g/cm³ | |
| Masa molar | 55,961 g/mol | |
| Punto de fusión | 679 K (406 °C) | |
| Punto de ebullición | 1593 K (1320 °C) | |
| Índice de refracción (nD) | 1,409, 1,421 | |
| Propiedades químicas | ||
| Solubilidad en agua | 119 g en 100 g de agua | |
| Termoquímica | ||
| ΔfH0gas | -232 kJ/mol | |
| ΔfH0líquido | -415,6 kJ/mol | |
| ΔfH0sólido | -425 kJ/mol | |
| S0sólido | 79 J·mol–1·K–1 | |
| Peligrosidad | ||
| NFPA 704 |
0
3
1
COR
| |
| Riesgos | ||
| Ingestión | Muy peligroso, puede causar daños permanentes, incluso la muerte. | |
| Inhalación | Muy peligroso, altas dosis pueden causar daños permanentes. Efectos debido a la exposición a largo plazo desconocidos. | |
| Piel | Causa quemaduras de diversos grado. | |
| Ojos | Causa quemaduras de diversos grado. | |
| LD50 | 273 mg/kg | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El hidróxido de potasio (también conocido como potasa cáustica) es un compuesto químico inorgánico de fórmula KOH, tanto él como el hidróxido de sodio (NaOH), son bases fuertes de uso común. Tiene muchos usos tanto industriales como comerciales. La mayoría de las aplicaciones explotan su reactividad con ácidos y su corrosividad natural. Se estiman en 700 000 a 800 000 toneladas la producción de hidróxido de potasio en 2005 (del NaOH se producen unas cien veces más).[2][3][4]
Propiedades y Estructura
El KOH es higroscópico y absorbe agua de la atmósfera por lo que termina por disolverse al aire libre. Por ello, el hidróxido de potasio contiene cantidades variables de agua (así como carbonatos, ver debajo). Su disolución en agua es altamente exotérmica, con lo que la temperatura de la disolución aumenta, llegando incluso, a veces, al punto de ebullición. Su masa molecular es de 56g/mol
Enlaces externos
Referencias
- ↑ Número CAS
- ↑ H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger “Potassium Compounds” in Ullmann’s Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. doi 039 10.1002/14356007.a22 039
- ↑ "Caustic Potash." Oxy.com Retrieved on January 24 2008.
- ↑ "Potassium Hydroxide." MSDS Retrieved on January 24

