Diferencia entre revisiones de «Hormona del crecimiento»
m Revertidos los cambios de 200.86.193.203 a la última edición de 190.232.90.138 |
|||
| Línea 115: | Línea 115: | ||
* [[Somatotropina]] |
* [[Somatotropina]] |
||
* [[Enanismo]] |
* [[Enanismo]] |
||
* [[Acromegalia]] |
* [[Acromegalia]] |
||
* [[Somatomedinas]] |
* [[Somatomedinas]] |
||
* [[Somatostatina]] |
* [[Somatostatina]] |
||
Revisión del 01:56 20 jul 2010

El sistema endocrino es un sistema de comunicación muy importante que se encarga de regular, coordinar e integrar gran cantidad de procesos fisiológicos. Lleva a cabo sus funciones mediante hormonas, que son sustancias químicas producidas por las células endocrinas como respuesta a estímulos específicos que regulan y coordinan las funciones fisiológicas ejerciendo sus acciones sobre células diana. Para llegar a éstas pueden secretarse directamente a la sangre o alcanzar las células por difusión en el líquido intersticial. Una vez se hayan puesto en contacto células diana y hormonas, éstas son reconocidas por receptores específicos en la membrana de las células. Es entonces cuando se desencadenan las distintas reacciones.
Hipófisis
La hipófisis (pituitaria) es una glándula que se encuentra en el diencéfalo unida al hipotálamo. Está dividida en dos lóbulos uno anterior (adenohipófisis) y uno posterior (neurohipófisis).
El lóbulo anterior es el que tiene verdadera actividad endocrina, está dividido en hipófisis anterior, con actividad endocrina, y la parte tuberal que se une al hipotálamo. Las hormonas segregadas por la hipófisis anterior reciben el nombre de hormonas tróficas aunque su función no sea de nutrición. Es así porque producen la hipertrofia de los órganos diana cuando se encuentran en grandes concentraciones y su atrofia cuando las concentraciones de éstas son bajas. Los nombres de las hormonas tróficas acaban con el sufijo -tropina.
Hormona del crecimiento
Composición química y producción de GH
La GH es el resultado de la expresión de una familia de genes formada por 5 miembros, y localizada en el cromosoma 17. Estos genes solo se expresan en las células de la pituitaria anterior (adenohipófisis), y una vez sintetizada la hormona en el retículo endoplasmático, se transporta mediante gránulos de secreción y es liberada ante un estímulo.
El hipotálamo es el encargado de controlar la secreción hipofisaria de GH, la regulación hipotalámica de la actividad endocrina de la adenohipófisis se realiza por vía hormonal a través de un sistema porta arterial (arteria hipofisaria superior). El hipotálamo secreta neurohormonas que llegan hasta la adenohipófisis vía sanguínea, GHIH y GHRH. Cuando segrega sobre la hipófisis un vertido de somatostatina (GHIH) provoca un efecto inhibidor tónico, que evita la formación de GH. Sin embargo, no es el cese del vertido de somatostatina lo único necesario para que tenga lugar la producción de GH, sino que el hipotálamo, también tiene que secretar la neurohormona liberadora de GH (GHRH). El resultado de esta secreción rítmica y aleatoria de somatostatina y GHRH es la liberación de GH en pulsos aleatorios que experimentan su mayor amplitud e importancia fisiológica durante el sueño.

Las células endocrinas de la adenohipófisis segregan seis hormonas peptídicas o polipeptídicas que se almacenan en gránulos secretores hasta que se recibe el factor de liberación y se produce la exocitosis a la sangre; entre ellas está la GH, producida por células acidófilas que forman el 50% d todas las células de la adenohipófisis. En algunos animales el porcentaje varía según el sexo. En ratas macho, representan el 30-40% de las células de la pituitaria, sin embargo en las hembras el valor desciende hasta 20-30%.
Somatotropina
La hormona del crecimiento (Growth Hormone, GH) es una cadena peptídica con dos puentes disulfuro internos formada por 191 aminoácidos con un peso molecular de 22.000 Da en humanos. Es la hormona que estimula el crecimiento de tejidos y órganos durante la niñez y adolescencia y continúa siendo importante durante toda la vida aunque haya cesado el crecimiento. No afecta al crecimiento fetal ni a los primeros meses de vida en gran cantidad.
Un déficit de GH en niños produce enanismo hipofisario y en exceso produce gigantismo. En adultos una deficiencia casi no tiene consecuencias aunque hay estudios que se remontan a 1992 que indican que un déficit en el adulto incrementa la morbilidad por accidentes cardiovasculares además de una variedad de síntomas tales como son el cansancio, intolerancia al ejercicio, acumulación de grasa abdominal entre otros; y el exceso, produce acromegalia que determina un aumento desproporcionado de las extremidades, dolores de cabeza y articulares y alteración de las proporciones faciales por aumento de las partes acras. El caso más curioso es el de Adam Rainer (1899) que a los 21 años medía 1’18m con lo cual fue considerado un enano. Pero a partir de ahí comenzó a crecer desmesuradamente, a los 32 medía 2’18m. Pasó de ser un enano a ser un gigante en tan sólo 12 años. Murió los 51 años con una altura de 2’34m. Por desgracia sólo existen teorías de las causas de este caso debido a la mala información y a las pocas técnicas científicas de la época.
Tiene efectos sobre muchos aspectos metabólicos. En anabolismo incrementa el balance positivo de nitrógeno, es decir, provoca la entrada de aminoácidos a las células y hace que éstos se incorporen a proteínas y en catabolismo estimula la obtención de energía de los lípidos y no de los glúcidos interviniendo así en la lipólisis del tejido adiposo. Además en periodos de ayuno, al ser segregada a la sangre disminuye el uso y almacenamiento de glucosa por los tejidos aumentando la concentración de glucosa en la sangre.
Tienes distintos efectos según el órgano o tejido diana:
| Órgano diana | Acción de la GH |
|---|---|
| Hueso | Estimula la diferenciación de las células precursoras del cartílago para que se conviertan en condrocitos (células maduras). Además estimula la mitosis y la actividad de los oseteoblastos (aumenta síntesis proteica, síntesis de ADN y ARN.) |
| Músculo | Aumenta la masa corporal ayudando a la captación de aminoácidos y síntesis de proteínas. |
| Tejido adiposo | Lleva a cabo lipólisis que disminuye la adiposidad. |
| Riñones y otros órganos | Aumenta su tamaño y por tanto su actividad. |
La GH actúa directamente sobre los tejidos adiposo, muscular y hepático. Pero muchas veces la hormona del crecimiento (GH) produce sus efectos anabólicos de forma indirecta estimulando otras glándulas para que produzcan las sustancias que se encargan de regular el crecimiento. Son las somatomedinas de las que hablaremos a continuación.
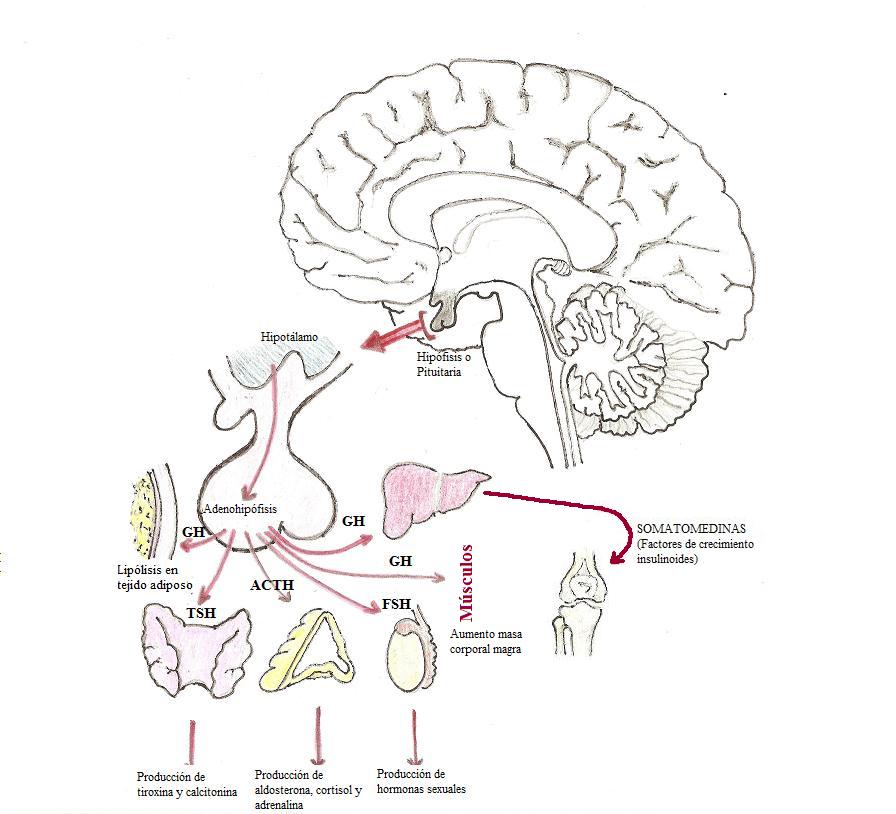
Regulación de la secreción de GH
La secreción de GH depende de la liberación intermitente de GHRH por el hipotálamo. Se segrega en pulsos cada dos horas, la mayor descarga se lleva a cabo durante el sueño. En niños y adolescentes la cantidad de GH circulando en la sangre es elevada, en adultos es menor. En cualquier caso sigue un ciclo circadiano, aumenta mientras dormimos y disminuye durante la vigilia.
La regulación de la secreción de GH depende, además del metabolismo, de factores hormonales y nerviosos.
| Factores | |
|---|---|
| Metabólicos | El ayuno, hipoglucemia por debajo del 50%, la hiponutrición y niveles bajos de ácidos grasos libres elevan la secreción de GH. Durante el ayuno, se degradan proteínas musculares y se consume glucosa, esto produce la secreción de un péptido gástrico estimulador de la GH (el Ghrelin)que aumenta los niveles de GH. |
| Hormonales | Las neurohormonas hipotalámicas: la GHRH (hormona liberadora de somatotropina) que se estimula con el hambre o el estrés y la GHIH (somatostatina) que inhibe la secreción de GH disminuyendo la sensibilidad de las células productoras de GH a la acción de la GHRH. Además otras hormonas estimulan la secreción de GH (hormonas sexuales, tiroideas y el cortisol) |
| Nerviosos | El ejercicio, el sueño profundo, los traumatismos, fiebre o cirugías elevan la concentración de GH en el plasma. |
Factores de regulación insulinoides (o somatomedinas)
A excepción del tejido adiposo, los músculos y el hígado a todas las demás células y órganos diana llegan péptidos producidos principalmente por los hepatocitos y que se parecen a la proinsulina; por ello reciben el nombre de Insulinlike Growth Factors (IGF) o Somatomedinas. Hay dos tipos, el IGF-1 con un 50% de homología con la insulina, incluso sus receptores de membrana son muy parecidos ya que producen autofosforilación, y el IGF-2 parecido en un 70% a la insulina y que por el contrario tiene receptores de membrana muy distintos a ésta. Sus funciones son estimular el crecimiento de los huesos y de los cartílagos, participar en la diferenciación de las células mesodérmicas y regular el metabolismo celular a nivel local.
El IGF-1 circula unido a un complejo de proteína mayor (IGF-Big Protein o IGF-BP), principalmente a la proteína fijadora de factor de crecimiento (IGF BP-3).Cuando la somatotropina estimula el hígado, este libera IGF-1 que se dirige hacia los órganos diana y actúa como una hormona. Pero en el cartílago, además de actuar como hormona, la IGF-1 actúa como regulador autocrino al estimular la división y el crecimiento celular (cuando la somatotropina estimula los condrocitos y estos liberan la IGF-1). Las somatomedinas no intervienen en el catabolismo de los lípidos ni en inhibir el uso de la glucosa.
Importancia de los factores de regulación insulinoides en el diagnóstico.
La GH no se puede detectar en el suero durante casi todo el día en pacientes sanos y no sometidos a estrés. Además si representamos gráficamente los valores de GH se observan unos picos discretos, que hacen muy difícil interpretar un valor aislado de la GH. Sin embargo, la IGF-I es constante a lo largo de todo el día, incluso después de la ingesta de alimentos. Por eso, son los valores de IGF-1 e IGF BP-3 los que se utilizan para diagnosticar y llevar a cabo un seguimiento de los pacientes con desórdenes en la función de la GH.

En humanos, los niveles de IGF-1 son prácticamente indetectables en el momento del nacimiento. Estos se elevan de manera gradual durante la infancia y su máximo valor se alcanza a la mitad de la adolescencia. Se mantienen medios hasta los 40 años aproximadamente, para después irse reduciendo de manera gradual. Un nivel bajo de IGF-1 es el valor más útil para diferenciar la condición normal de la deficiencia de Hormona del Crecimiento cuando la deficiencia es severa. También es utilizada para evaluar el cambio del estado nutricional.
En el mantenimiento de la masa muscular-esquelética y en la hipertrofia de ésta, se manifiesta el rol central de IGF-1 y se ha planteado que la falta de IGF-1 sea una de las principales causas por las que el músculo esquelético pierde masa y fuerza con el transcurso de la edad.
Producción de GH sintética
Para tratar las afecciones por deficiencia de somatotropina se han creado, de distintas maneras, hormonas sintéticas estructuralmente idénticas a la GH para que sus efectos sean más precisos. Los medios utilizados para fabricar y purificar somatotropina son un factor muy importante a tener en cuenta. Entre ellos están:
- Somatotropina / Cadáver-HC
El uso de la Hormona del crecimiento Cadáver fue aprobado como tratamiento para el déficit de hormona de crecimiento desde los años 60 hasta los 80. La Cadáver-HC se obtiene purificando la hormona de crecimiento recogida del páncreas de cadáveres. Sin embargo, en los 80, se descubrió que el mal de Creutzfeld-Jakob (MCJ) puede ser transferido desde los cadáveres a los usuarios, y su uso fue suspendido.
- El Somatrem / Tecnología Inclusion Body / Met-HCH
Met- HCH fue la primera forma biosintética de hormona del crecimiento humana que se desarrolló. Pero como Met-HC no era hormona de crecimiento pura, produjo efectos colaterales. Esto es debido a que Met-HC tiene un aminoácido metionil adicional que provoca que la persona genere anticuerpos en su contra. Algunos usuarios sufrieron reacciones alérgicas al Met-HC y en otros produjeron tanta resistencia, que neutralizaron su efecto.
- La Somatotropina / Tecnología Protein Secretion y Fabricación Mouse-Cell / HCH
El método de fabricación GH más comúnmente utilizado a día de hoy es a través de tecnología Protein Secretion o de fabricación Mouse-cell. Los dos métodos crean una hormona del crecimiento idéntica a la GH producida de forma natural por el cuerpo humano.
- Sprays y Píldoras de HCH
Muchas compañías interesadas en acrecentar su economía gracias a la industria de esta hormona han fabricado un spray de hormonas del crecimiento vegetales, asegurando al cliente mayor efectividad a menor coste que la GH inyectable. Sin embargo, no es para nada cierto debido a que la GH es un polipéptido frágil y de gran tamaño (22.000Da) que contiene 191 aminoácidos en una secuencia exacta, y con determinadas uniones que le dan una configuración 3-D imprescindible para su funcionamiento. La única forma segura de fabricar una GH correcta es empalmando genes humanos con bacterias o con células madre, y haciendo crecer esas células. No hay en absoluto ninguna fuente vegetal de HCH. La HCH debe ser producida utilizando genes humanos.
- Fermentación a altas densidades de E. coli recombinante 4, para la obtención de GH
En este método se utiliza la bacteria E. coli (cepa: K802) como lugar de hospedaje para el plásmido que codifica la hormona del crecimiento humana (plásmido: SSM). Luego se cultiva la cepa modificada para lo cual se inocula en un medio LB a pH 7, y como fuente de carbono se le añade glicerol en lugar de glucosa, disminuyendo así el tiempo de fermentación y evitando la producción de subproductos como el acetato que inhibe el crecimiento de la comunidad bacteriana. Las E. coli cultivadas se trasladan a un tanque con 200 ml del medio de LB y 100mg/ml de ampicilina y lo mantenemos incubando 12 horas a 37 °C. Tras este periodo de incubación, centrifugamos a 220 rpm. Finalmente, extraemos la hormona acumulada de manera intracelular. Este método ha logrado varias ventajas mejorando la productividad, reduciendo el volumen utilizado y los costos tanto de producción como de inversión en equipo.
Enlaces internos
Bibliografía
-MARTIN CUENCA, E. "Fundamentos de fisiología" Ed. Thomson (2006)
-RHOADES, R. A.; TANNER, G. A. "Fisiología médica" eD. Elsevier (1997)
-Artículo: “Acromegalia, envidia a las alturas” [1]


