Ácido brómico
Apariencia
| Ácido brómico | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| Ácido trioxobrorómico (V) | ||
| General | ||
| Otros nombres | Trioxobromato (V) de hidrógeno | |
| Fórmula semidesarrollada | HBrO3 | |
| Fórmula estructural |
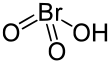 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 7789-31-3[1] | |
| Número RTECS | TP8580000 | |
| ChEBI | 49382 | |
| ChemSpider | 22853 | |
| PubChem | 24445 | |
| UNII | 908X3OZ87J | |
| Propiedades físicas | ||
| Masa molar | 128,91 g/mol | |
| Propiedades químicas | ||
| Momento dipolar | 0 D | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El ácido brómico (HBrO3) es un oxácido del bromo, cuyo estado de oxidación es 5. Es poco estable y solo puede disponerse en solución acuosa,[2][3] pues se descompone con relativa facilidad si se intenta concentrar. Esto hace, que incluso las disoluciones diluidas de este ácido, inicialmente incoloras, a temperatura ambiente cambien lentamente a color marrón debido a la presencia de bromo molecular.[4]Tanto el ácido brómico como sus cales, los bromatos, son poderosos agentes oxidantes, al igual que los cloratos.
Contiene aproximadamente 62% de bromo, 1 % de hidrógeno y 37% de oxígeno.
Referencias[editar]
- ↑ Número CAS
- ↑ Van Nostrand's Scientific Encyclopedia. Glenn D. Considine. Ninth Edition. Volume 1. p 554
- ↑ The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals. 14th Edition. 2006.
- ↑ Recipes for Belousov–Zhabotinsky reagents. J. Chem. Educ., 1991, 68 (4), 320. doi:10.1021/ed068p320
