Ebastina
| Ebastina | ||
|---|---|---|
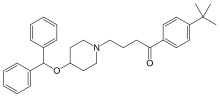 | ||
| Nombre (IUPAC) sistemático | ||
|
4-(4-benzhydryloxy-1-piperidyl)-1- (4-tert-butylphenyl)butan-1-one | ||
| Identificadores | ||
| Número CAS | 90729-43-4 | |
| Código ATC | R06 | |
| PubChem | 3191 | |
| Datos químicos | ||
| Fórmula | C32H39NO2 | |
| Peso mol. | 469,658 g/mol | |
| Farmacocinética | ||
| Unión proteica | Mayor del 95% | |
| Metabolismo | Hepático (CYP3A4-mediado) | |
| Vida media | 15 a 19 horas | |
| Datos clínicos | ||
| Vías de adm. | Oral | |
La ebastina es un antihistamínico H1, de segunda generación.
Introducción
[editar]La ebastina es un antagonista H1 de segunda generación que está indicado para la rinitis alérgica y la urticaria idiopática crónica. Está disponible en tabletas de 10 y 20 mg, en su nueva formulación de tabletas de disolución rápida de 10 y 20 mg y en jarabe pediátrico. Con una dosis flexible recomendable de 10 o 20 mg dependiendo de la gravedad de la afección.
La ebastina está disponible en diferentes presentaciones (tabletas, tabletas de disolución rápida y jarabe) y se comercializa en todo el mundo bajo diferentes nombres, Ebastel, Ebastel FLAS, Kestine, KestineLYO, Evastel Z, Alerno, etc.
Perfil Farmacocinético
[editar]Estructura química y molecular
Ebastina: • Segunda generación H1, bloqueador de los receptores • C32 H39 NO2 • 4-difenilmetoxi-1-(3-[4-terbutilbenzoil]-propil) piperidina • Peso molecular 469,62
El metabolito activo de la ebastina es la carebastina con una tasa de conversión del 100%
La ebastina tiene una estructura química única que se diferencia de otros antihistamínicos de segunda generación. Después de administrarse de forma oral, a través del citocromo P450 3A4 experimenta un primer paso metabólico en su metabolito activo del ácido carboxílico, la carebastina. Con una tasa de conversión del 100%.
No es necesario ajustar la dosis en ancianos ni en caso de pacientes con insuficiencia renal ni en pacientes con insuficiencica hepática de leve a moderada.

Eficacia
[editar]Los resultados obtenidos en más de 8.000 pacientes de más de 40 estudios clínicos sugiere la eficacia de la ebastina en el tratamiento intermitente de rinitis alérgica, rinitis alérgica persistente y en otras indicaciones.
Seguridad
[editar]La ebastina ha mostrado un perfil de tolerabilidad y seguridad total. Los efectos adversos más frecuentes fueron comparables a los que presentaron los pacientes de los grupos placebos durante la fase del desarrollo clínico, lo que confirma que ebastina tiene un muy buen perfil de seguridad.
Ebastina 10 y 20 mg se puede administrar a adultos y a niños mayores de 12 años ya que ya consta el jarabe pediátrico.
Ebastina debe usarse durante el embarazo solo si es necesario.
Interacciones:
Toda la información está incluida en la referencias bibliográficas, especialmente la 5 y la 10.
Comprimidos de disolución rápida
[editar]Los comprimidos liofilizados se disuelven con rapidez en la boca y los pacientes tienen la percepción de una más rápida acción anthistamínica comparada con la de las convencionales. Han demostrado una bioequivalencia farmacocinética con las formulaciones convencionales y un perfil farmacodinámico superior al de otros anthistamínicos habituales. Los pacientes valoran la nueva formulación por su comodidad y la percepción de mayor rapidez de acción.[cita requerida]
Los comprimidos de ebastina disolución rápida contienen aspartamo. Los pacientes que padezcan fenilcetonuria deben tenerlo en cuenta.
Bibliografía
[editar]- Peyri, J.; Vida, J.; Marrón, J.; Fonseca, E.; Suárez, E.; Ledo, A.; Zayas, J. M.; Luria, X. (1991). «Ebastine in chronic urticaria: A double-blind placebo-controlled study». Journal of Dermatological Treatment 2 (2): 51-53. doi:10.3109/09546639109086774.
- Gehanno, Pierre; Bremard-Oury, Clothilde; Zeisser, Philippe (1996). «Comparison of Ebastine to Cetirizine in Seasonal Allergic Rhinitis in Adults». Annals of Allergy, Asthma & Immunology 76 (6): 507-512. doi:10.1016/S1081-1206(10)63269-3.
- Bousquet, J; Gaudaño, Em; Palma Carlos, Ag; Staudinger, H (1999). «A 12-week, placebo-controlled study of the efficacy and safety of ebastine, 10 and 20 mg once daily, in the treatment of perennial allergic rhinitis». Allergy 54 (6): 562-568. doi:10.1034/j.1398-9995.1999.00984.x.
- Tagawa, Masaaki; Kano, Michiko; Okamura, Nobuyuki; Higuchi, Makoto; Matsuda, Michiaki; Mizuki, Yasuyuki; Arai, Hiroyuki; Iwata, Ren; Fujii, Toshihiko; Komemushi, Sadao; Ido, Tatsuo; Itoh, Masatoshi; Sasaki, Hidetada; Watanabe, Takehiko; Yanai, Kazuhiko (2001). «Neuroimaging of histamine H1-receptor occupancy in human brain by positron emission tomography (PET): A comparative study of ebastine, a second-generation antihistamine, and (+)-chlorpheniramine, a classical antihistamine». British Journal of Clinical Pharmacology 52 (5): 501-509. doi:10.1046/j.1365-2125.2001.01471.x.
- Van Cauwenberge, Paul; De Belder, Tine; Sys, Lien (2004). «A review of the second-generation antihistamine ebastine for the treatment of allergic disorders». Expert Opinion on Pharmacotherapy 5 (8): 1807-1813. doi:10.1517/14656566.5.8.1807.
- Ratner, P.; Falqués, M.; Chuecos, F.; Esbrí, R.; Gispert, J.; Peris, F.; Luria, X.; Rosales, M.J. (2005). «Meta-Analysis of the Efficacy of Ebastine 20 mg Compared to Loratadine 10 mg and Placebo in the Symptomatic Treatment of Seasonal Allergic Rhinitis». Int Arch Allergy Immunol 138 (4): 312-318. doi:10.1159/000088869.
- Antonijoan, Rosa M.; García-Gea, Consuelo; Puntes, Montserrat; Valle, Marta; Esbri, Ramon; Fortea, Josep; Barbanoj, Manuel J. (2007). «A Comparison of Ebastine 10mg Fast-Dissolving Tablet with Oral Desloratadine and Placebo in Inhibiting the Cutaneous Reaction to Histamine in Healthy Adults». Clinical Drug Investigation 27 (7): 453-461. doi:10.2165/00044011-200727070-00002.
- Antonijoan, Rosa; García-Gea, Consuelo; Puntes, Montserrat; Pérez, Joselin; Esbrí, Ramón; Serra, Cristina; Fortea, Josep; Barbanoj, Manuel J. (2007). «Comparison of inhibition of cutaneous histamine reaction of ebastine fast-dissolving tablet (20 mg) versus desloratadine capsule (5 mg): A randomized, double-blind, double-dummy, placebo-controlled, three-period crossover study in healthy, nonatopic adults». Clinical Therapeutics 29 (5): 814-822. doi:10.1016/j.clinthera.2007.05.001.
- Salvà, M; Carreño, B; Pintos, M (2004). «Phase I, single dose, open label, randomized, crossover bioequivalence studies of ebastine 10 mg and 20 mg regular tablets vs 10 and 20 mg fast-dissolving tablets in healthy male volunteers». J Invest Allergol Clin Immunol 14 (4 (Suppl 1)): S5.
- Sastre, J. (2008). «Ebastine in allergic rhinitis and chronic idiopathic urticaria». Allergy 63 (Suppl. 89): 1-20. doi:10.1111/j.1398-9995.2008.01897.x.
El número de INN es 5633.
